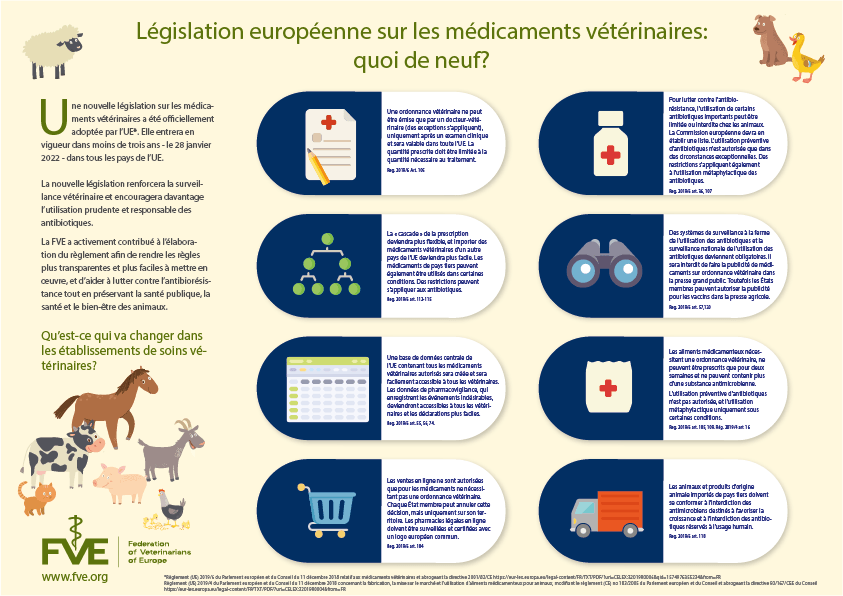
Ouverture du marché du médicament vétérinaire : qu'est-ce qui va changer en 2022 ?
La Commission européenne veut renforcer la lutte contre les maladies animales, tout en limitant la résistance aux antibiotiques. Elle a adopté une nouvelle réglementation, qui va faire bouger les lignes du marché du médicament vétérinaire. Explications avec Arnaud Deleu, directeur des affaires économiques et de la formation au Syndicat de l’industrie de la santé animale, SIMV.
Le marché des médicaments vétérinaires en pleine évolution
Arnaud Deleu, directeur des affaires économiques et
de la formation au Syndicat de l’industrie de la santé
animale, SIMV
Le 28 janvier 2022, le marché des médicaments vétérinaires connaîtra un nouveau paysage du fait de l’évolution de la réglementation européenne. « L’ambition de la Commission est de renforcer la disponibilité du médicament vétérinaire et lutter contre l’antibiorésistance, explique Arnaud Deleu, directeur des affaires économiques et de la formation au Syndicat de l’industrie de la santé animale, SIMV. Pour cela, elle souhaite faciliter la vente des médicaments dans toute l’Union et éviter des situations d’impasse.»
Concrètement, le règlement 2019/6 abroge la directive 2001/82 qui constitue, avec le règlement 726/2004, le cadre réglementaire actuel de l’Union européenne sur l’utilisation des médicaments vétérinaires.
Pas moins de 160 articles composent le texte. Lequel instaure un cadre règlementaire européen unique en matière d’autorisation de mise sur le marché, AMM, des médicaments vétérinaires. Le règlement comprend des champs aussi larges que l’étiquetage et la notice, les bases de données, la pharmacovigilance, la fabrication, l’importation et l’exportation, la distribution en gros et la vente au détail physique ou via Internet, la prescription, la publicité et la promotion, mais également l’inspection, les contrôles ainsi que les sanctions.
Faciliter la diffusion des médicaments dans l'Union Européenne
Quels sont les principaux changements ? Une certaine partie du texte concerne la distribution en gros. Les autorisations demeurent octroyées par les autorités nationales, mais elles seront valables dans toute l’UE. Actuellement, les ventes entre les États membres requièrent des accords de reconnaissance mutuelle entre pays. Ce point entend donc faciliter la commercialisation des médicaments dans l’UE. Corollaire de cette ouverture, les bonnes pratiques de distribution, ou BPD, deviennent communes à tous les pays. « La France a déjà mis en place toutes ces pratiques, ce point ne va donc pas engendrer de contraintes supplémentaires », ajoute le directeur des affaires économiques du SIMV.
Par ailleurs, les règles de vente au détail physique de médicaments vétérinaires sont déterminées par le droit national et ne devraient pas évoluer en France.
Un cadre pour Internet
En revanche, les ventes sur Internet disposent désormais d’un cadre, fournit par l’article 104.
« Aucune réglementation n’existe actuellement, indique Arnaud Deleu. Cela est donc bienvenue. » Cette vente est réservée aux détaillants autorisés pour la vente « physique » et concerne les médicaments non soumis à prescription. Pour ceux soumis à prescription, chaque pays a la liberté d’autoriser la commercialisation via Internet. Elles sont alors limitées au territoire national.
Seul un vétérinaire peut prescrire des médicaments vétérinaires. « Les pays pouvaient précédemment confier cette disposition à d’autres intervenants, mais cette pratique n’existe pas en France », précise-t-il.
Une cascade réduite
Les règles de la cascade sont revues et cadrées par les articles 112 à 114. Le nombre d’étapes devient inférieur à ce qui existe actuellement. Objectif : délivrer plus rapidement un médicament. Plusieurs cas sont prévus. S’il n’existe pas de médicament pour une cause précise, le vétérinaire peut traiter les animaux ne produisant pas de denrée alimentaire avec un médicament autorisé chez toute espèce animale, quelle que soit l’indication. À défaut, il peut choisir un médicament à usage humain autorisé, ou à défaut un médicament vétérinaire en préparation extemporanée conforme aux termes d’une ordonnance vétérinaire.
Une étape est ajoutée dans cette cascade pour les animaux producteurs de denrées. Ainsi lorsqu’il n’existe pas de médicament, le vétérinaire peut traiter les animaux avec un médicament autorisé pour animaux qui produisent des aliments pour la même indication ou pour une autre. Si cela n’existe pas, il pourra piocher dans les médicaments autorisés chez une espèce animale non productrice de denrées alimentaires, ou à défaut chez l’homme puis une préparation extemporanée.
Les temps d’attente maximaux pour la consommation des aliments issus des animaux traités avec des médicaments utilisés en dehors des termes de l’AMM sont également revus, et ce par filière, via l’article 115. Par exemple, pour le lait, il correspond au temps d’attente le plus long indiqué dans les caractéristiques du produit pour n’importe quelle espèce animale, multiplié par 1,5. Il est fixé à sept jours si le médicament n’est pas autorisé pour les animaux producteurs de lait pour la consommation humaine, et à un jour s’il est nul.
Publicité et pharmacovigilance renforcée
Les États pourront également autoriser la publicité des médicaments à destination des éleveurs professionnels. « Avant, cette publicité était destinée aux ayants droits, explique Arnaud Deleu. Maintenant il est possible de communiquer auprès des agriculteurs afin de les sensibiliser et éviter les traitements curatifs. C’est d’ailleurs le choix de la France.»
Enfin la pharmacovigilance est renforcée avec la mise en place d’un système de détection du signal, la surveillance en continu du post-AMM, ou encore l’accès public à la base de données de l’Union en la matière.
S’agissant d’un règlement, le texte sera directement applicable le 28 janvier 2022 sans transposition. Toutefois, la France s’est laissée un délai supplémentaire jusqu’au 3 mars dans le cadre de la loi n°2020-1508. «Le gouvernement a promis de le faire avant et d’être près en temps et en heure », précise Arnaud Deleu.
Les conséquences de cette évolution sont encore floues. « Il est difficile de les anticiper, reconnaît-il. Mais, la France répond déjà à de nombreux points de cette nouvelle réglementation et les opérateurs ne devraient pas trop s’inquiéter. De plus, la distribution nationale est très efficace, avec une gamme la plus riche d’Europe contenant plus de 3000 AMM. La France pourrait même tirer son épingle du jeu. »
Ouverture du marché du médicament vétérinaire : le récap